疾患解説
ANCA関連血管炎(ANCA associated vasculitis、AAV)
1. 疾患概念と疫学
ANCA関連血管炎(ANCA associated vasculitis、AAV)とは、血清中のANCA(抗好中球細胞質抗体、anti-neutrophil cytoplasmic antibody)陽性を特徴とする小型血管炎であり、下記に分類される。
- 顕微鏡的多発血管炎(microscopic polyangiitis、MPA)
- 多発血管炎性肉芽腫症(granulomatosis with polyangiitis、GPA、旧:Wegener肉芽腫症)
- 好酸球性多発血管炎性肉芽腫症(eosinophilic granulomatosis with polyangiitis、EGPA、旧:Churg Strauss症候群)
名称にANCAが含まれるもののANCA陰性例も存在する。ANCAの陽性率は、報告・疾患にもよるが、MPAで70%、GPAで80-90%、EGPAで50%などと報告されている。遺伝学的には、疾患の分類よりANCAのタイプにより背景となる遺伝子素因が異なり、PR3-ANCA陽性例ではHLA-DP, SERPINA1, PRTN3との関連、MPO-ANCA陽性例ではHLA-DQとの関連が報告されている(Lyons PA, et al. N Eng J Med. 2012. 367:214-23)。
ANCAの対応抗原は好中球が活性化された際に放出されるNeutrophil extracellular traps (NET)の構成成分に含まれており、自己抗体の出現には、何らかの刺激によるNETosisの亢進の関与が想定されている。薬剤関連のANCA関連血管炎も存在し、サルファ剤、抗不整脈薬などが原因として報告されている。これらの薬剤のうち、NETosisを誘導するものがあり、発症機序として注目されている。
AAVの疫学は欧米と日本で大きく異なり、欧米ではGPA、PR3-ANCA陽性例が多いのに対して、日本ではMPA、MPO-ANCA陽性例が多い。また、日本人AAVの方が、平均発症年齢が高い。日本における年間発症率は22.6/millionで、81%がMPA、10%がEGPA、9%がGPA、平均発症年齢は69.7歳と報告されている。男女比に関しては、女性が51.2%と女性にやや多い。高齢発症の症例では、よりMPAの割合が高い。
2. 臨床症状
小型血管炎で共通して見られることが多い症状としては、肺胞出血、腎障害(急性進行性糸球体腎炎)、多発単神経炎、皮疹(livedo reticularisやpalpable purpuraなど)が挙げられる。その他、発熱、全身倦怠感、体重減少などの全身症状は、いずれでも見られ得る。
MPAでは、腎障害(91%)、肺病変(39%)、末梢神経障害(42%)の頻度が高い。GPAでは、①E:上気道(鼻中隔穿孔・鼻出血・副鼻腔炎・中耳炎など)、②L:肺(血痰・結節影など)、③K:腎の症状が、E→L→Kの順で出現することが多いとされている。EGPAでは、気管支喘息やアレルギー性鼻炎などのアレルギー症状が先行した後に、末梢血好酸球増多、血管炎に伴う症状が出現する。EGPAの血管炎に伴う臓器病変としては、多発単神経炎、皮疹、虚血性腸炎が多い。
以下に各疾患において見られる頻度の高い臓器病変を示すKlippel JH. Primer on the Rheumatic Diseases. 13 ed: Springer; 2008.より改変)。
AAVで頻度の高い臓器障害
| GPA | MPA | EGPA | |
|---|---|---|---|
| 耳鼻咽喉 領域 |
鼻中隔穿孔、鞍鼻、難聴、声門下狭窄 | まれ | 鼻ポリープ、アレルギー性鼻炎、伝音性難聴 |
| 眼 | 眼窩内腫瘤、強膜炎、上強膜炎、ぶどう膜炎 | まれ | まれ |
| 肺 | 結節影、浸潤影、空洞性病変、肺胞出血 | 肺胞出血、間質性肺炎 | 気管支喘息、好酸球性肺炎、肺胞出血 |
| 腎 | 急性進行性糸球体腎炎 | 急性進行性糸球体腎炎 | 急性進行性糸球体腎炎 |
| 心臓 | 弁病変 | まれ | 心不全、心膜炎、不整脈 |
| 末梢神経 | 多発単神経炎 | 多発単神経炎 | 多発単神経炎 |
| 皮膚 | 皮下結節、紫斑、潰瘍など | 紫斑など | 皮下結節、紫斑、潰瘍など |
| 消化管 | まれ | 虚血性腸炎 | 好酸球性胃腸炎、虚血性腸炎 |
上記以外にも、肥厚性硬膜炎や脳神経障害、下垂体病変など多彩な病変が報告されている。
3. 検査
疾患、個々の症例によって、臓器病変の広がりが異なるため、病歴・身体所見・一般検査所見から、臓器病変の広がりを推測し、その有無と重症度を評価する。診断に当たっては、組織学的検査が重要である。また、他疾患を除外するための検査も並行して行う。
1) ANCAについて
ANCAは好中球に対する自己抗体であり、当初間接蛍光抗体法の染色パターンから、細胞質がびまん性に染まるcytoplasmic ANCA(C-ANCA)と核周辺が強く染まるperipheral ANCA(P-ANCA)に分類されていた。その後、それらの主な対応抗原が、proteinase 3(PR3)、myeloperoxidase(MPO)であることが判明し、現在は、ELISAやCLEIA法で、これらの抗原に対する抗体(PR3-ANCA、MPO-ANCA)を測定することが一般的となっている。教科書的には、GPAではPR3-ANCA陽性例が多く、MPAとEGPAがMPO-ANCA陽性が多いとされているが、日本のGPAにはMPO-ANCA陽性例が半数程度存在する。
2)その他の採血項目:血算(分画含む)、生化学(TP、Alb、BUN、Cre、肝機能、CRPなど)、RF、血沈
3)臓器別の評価:なるべく生検を行い、組織学的診断をつけるようにする
- 頭頸部病変の評価:頭部CT・MRI、眼科診察、耳鼻科診察、病変部位の生検
- 肺病変の評価:胸部X線、胸部CT、KL-6、SP-D、動脈血ガス、呼吸機能検査、気管支鏡、経気管支肺生検(TBLB)、外科的肺生検(VATS)
- 腎病変の評価:尿定性、沈渣、尿生化学、腎生検
- 皮膚病変の評価:皮膚科診察、皮膚生検
- 神経病変の評価:神経内科診察、神経伝導速度検査、腓腹神経生検、頭部MRI
- そのほか:心エコー、ホルター心電図、便潜血、GF、CFなど
4.診断基準・分類基準
AAVの診断基準・分類基準の主なものには下記がある。
1)1990年ACR分類基準:臨床研究における分類基準として使用されることを念頭に、1990年他の血管炎とともにGPA、EGPAの分類基準がアメリカリウマチ学会から提唱された( Leavitt RY, et al. Arthritis Rheum. 1990;33:1101-7., Masi AT, et al. Arthritis Rheum. 1990;33:1094-100.)。MPAの疾患概念が確立する前でありMPAの分類基準がないこと、またANCAの測定が一般的となる前であり分類基準に含まれていないことなどが問題点として挙げられている。
・EGPAの分類基準(ACR、1990年)
①喘息
②好酸球増多症(白血球分画の10%以上)
③単神経障害あるいは多発神経炎
④肺浸潤影
⑤副鼻腔異常
⑥血管外組織への好酸球浸潤の6項目中4項目を満たす場合にEGPAと分類する。
・GPAの分類基準(ACR、1990年)
①鼻または口腔内の炎症:有痛性あるいは無痛性口腔内潰瘍、または化膿性あるいは血性鼻汁の出現
②胸部レントゲン異常影: 結節、空洞、あるいは固定性浸潤
③尿沈渣異常: 顕微鏡的血尿(>5 RBC/HPF)あるいは赤血球円柱
④生検における肉芽腫性炎症の証明: 動脈壁、血管周囲または血管外領域(動脈、小動脈)に肉芽腫を認めるの4項目のうち2項目を満たす場合にGPAと分類する。
2)Chapel Hill Consensus Conference criteria :それぞれの血管炎を定義することを目的としている。分類基準や診断基準ではない。1994年に作成され、2012年に改訂された(別項参照) 。
3)EMA algorithm(Wattsらのalgorithm):上記のACR基準の問題点を受けて、主に疫学研究での使用を念頭にMPAの疾患概念が確立した後に提唱されたアルゴリズム。ACRの分類基準やLanhamの基準、CHCCの定義、ANCAなどのsurrogate markerを用いて、classification treeに沿って、EGPA、GPA、MPA、PANの順に順次症例を分類していく。 (Watts R, et al. Ann Rheum Dis. 2007;66:222-7.)
EMAアルゴリズム( 尾崎ら. ANCA関連血管炎の診療ガイドライン2011. より転載)
GPAのSurrogate markers
下気道 レントゲンでの肺浸潤影、結節影、空洞影、気管支狭窄 上気道 血清鼻汁、鼻粘膜潰瘍、慢性副鼻腔炎、中耳炎、乳様突起炎、眼窩腫瘤、声門下狭窄、鞍鼻、破壊性副鼻腔炎4)厚生労働省の基準:本邦における臨床現場における診断基準として、MPA、GPA、EGPAそれぞれの診断基準が提唱されている。難病情報センターホームページ. Available from: www.nanbyou.or.jp.
5)活動性の評価としては、Birmingham Vasculitis Activity Score (BVAS)が有名である。
Birmingham Vasculitis Activity Score (version 3)
Patient ID: Date of birth: Total score:
Assessor: Date of assessment
Tick an item only if attributable to active vasculitis. If there are no abnormalities in a section, please tick ‘None’ for that organ-system. |
If all abnormalities are due to persistent disease (active vasculitis which is not new/worse in the prior 4 weeks), tick the PERSISTENT box at the bottom right corner |
||||
Is this the patient’s first assessment? |
Yes ○ |
||||
None |
Active disease |
|
None |
Active disease |
|
|---|---|---|---|---|---|
1. General |
○ |
|
6. Cardiovascular |
○ |
|
Myalgia |
○ |
Loss of pulses |
○ |
||
Arthralgia / arthritis |
○ |
Valvular heart disease |
○ |
||
Fever ≥38° C |
○ |
Pericarditis |
○ |
||
Weight loss ≥2 kg |
○ |
Ischaemic cardiac pain |
○ |
||
2. Cutaneous |
○ |
|
Cardiomyopathy |
○ |
|
Infarct |
○ |
Congestive cardiac failure |
○ |
||
Purpura |
○ |
7. Abdominal |
○ |
|
|
Ulcer |
○ |
Peritonitis |
○ |
||
Gangrene |
○ |
Bloody diarrhoea |
○ |
||
Other skin vasculitis |
○ |
Ischaemic abdominal pain |
○ |
||
3. Mucous membranes / eyes |
○ |
|
8. Renal |
○ |
|
Mouth ulcers |
○ |
Hypertension |
○ |
||
Genital ulcers |
○ |
Proteinuria >1+ |
○ |
||
Adnexal inflammation |
○ |
Haematuria ≥10 RBCs/hpf |
○ |
||
Significant proptosis |
○ |
Serum creatinine 125-249 µmol/L* |
○ |
||
Scleritis / Episcleritis |
○ |
Serum creatinine 250-499 µmol/L* |
○ |
||
Conjunctivitis / Blepharitis / Keratitis |
○ |
Serum creatinine ≥500 µmol/L* |
○ |
||
Blurred vision |
○ |
Rise in serum creatinine >30% or fall in creatinine clearance >25% |
○ |
||
Uveitis |
○ |
*Can only be scored on the first assessment |
|||
Retinal changes (vasculitis / thrombosis / exudate / haemorrhage) |
○ |
9. Nervous system |
○
|
○ |
|
4. ENT |
○ |
Organic confusion |
○ |
||
Bloody nasal discharge / crusts / ulcers / granulomata |
○ |
Seizures (not hypertensive) |
○ |
||
Paranasal sinus involvement |
○ |
Spinal cord lesion |
○ |
||
Subglottic stenosis |
○ |
Cranial nerve palsy |
○ |
||
Conductive hearing loss |
○ |
Sensory peripheral neuropathy |
○ |
||
Sensorineural hearing loss |
○ |
Mononeuritis multiplex |
○ |
||
5. Chest |
○ |
|
|
||
Wheeze |
○ |
10. Other |
○ |
||
Nodules or cavities |
○ |
a. |
○ |
||
Pleural effusion / pleurisy |
○ |
b. |
○ |
||
Infiltrate |
○ |
c. |
○ |
||
Endobronchial involvement |
○ |
d. |
○ |
||
Massive haemoptysis / alveolar haemorrhage |
○ |
PERSISTENT DISEASE ONLY: |
□ |
||
References:
Version 1: Luqmani, RA, et al. (1994). "Birmingham Vasculitis Activity Score (BVAS) in systemic necrotizing vasculitis." QJM 87(11):671-8.
Version 2: Luqmani, RA, et al. (1997). "Disease assessment and management of the vasculitides." Baillieres Clin Rheumatol 11(2): 423-46.
Version 3: Mukhtyar C, et al (2008). "Modification and validation of the Birmingham Vasculitis Activity Score (version 3) (unpublished)
GLOSSARY AND SCORING FOR BVAS version 3
Rules for scoring BVAS
- Disease manifestations are scored only when they are attributable to active vasculitis. The manifestation should not be scored if there is reasonable evidence of another aetiology for the symptoms e.g. infection, drug reaction, other co-morbidity.
- Tick "Persistent Disease" box if all the abnormalities are due to active (but not new or worse) vasculitis.
- Specialist opinion, or the results of laboratory or imaging investigations will be required for some items. Excepting those circumstances, the whole form should be completed at the time of the consultation.
- The bands of serum creatinine should be scored only on the first visit.
Items marked with an asterisk (*) are not compatible with ‘persistent’ disease. These manifestations always suggest new or worse disease when due to active vasculitis.
| Manifestation | Definition | Persistent | New / Worse |
|---|---|---|---|
| 1. General | Maximum scores | 2 |
3 |
| Myalgia | Pain in the muscles | 1 |
1 |
| Arthralgia or arthritis | Pain in the joints or joint inflammation | 1 |
1 |
| Fever ≥38° C | Documented oral / axillary temperature. If rectal temperature is measured, raise threshold to 38.5° C | 2 |
2 |
| Weight Loss ≥2 kg | Loss of dry body weight without dieting | 2 |
2 |
| 2. Cutaneous | Maximum scores | 3 |
6 |
| Infarct | Area of tissue necrosis or splinter haemorrhages | 1 |
2 |
| Purpura | Subcutaneous or submucosal haemorrhage in the absence of trauma | 1 |
2 |
| Ulcer | A disruption in the continuity of the skin | 1 |
4 |
| Gangrene | Extensive tissue necrosis | 2 |
6 |
| Other skin vasculitis | Livedo reticularis, subcutaneous nodules, erythema nodosum, etc | 1 |
2 |
| 3. Mucous Membranes / eyes |
Maximum scores | 3 |
6 |
| Mouth ulcers / granulomata | Aphthous stomatitis, deep ulcers, strawberry gingival hyperplasia | 1 |
2 |
| Genital ulcers | Ulcers on the genitalia or perineum | 1 |
1 |
| Adnexal inflammation | Salivary or lacrimal gland inflammation. | 2 |
4 |
| Significant proptosis | >2 mm protrusion of the eyeball | 2 |
4 |
| Scleritis / Episcleritis | Inflammation of the sclera | 1 |
2 |
| Conjunctivitis / Blepharitis / Keratitis | Inflammation of the conjunctiva, eyelids or cornea - but not due to sicca syndrome | 1 |
1 |
| Blurred vision | Deterioration of visual acuity from previous or baseline | 2 |
3 |
| Sudden visual loss* | Acute loss of vision | * |
6 |
| Uveitis | Inflammation of the uvea (iris, ciliary body, choroid) | 2 |
6 |
| Retinal changes (vasculitis, thrombosis / exudate / haemorrhage) | Sheathing of retinal vessels or evidence of retinal vasculitis on fluorescein angiography; thrombotic retinal arterial or venous occlusion; soft retinal exudate (exclude hard exudates) / retinal haemorrhage | 2 |
6 |
| 4. ENT | Maximum scores | 3 |
6 |
| Bloody nasal discharge / crusts / ulcers / granulomata | Bloody, mucopurulent, nasal secretion, light or dark brown crusts frequently obstructing the nose, nasal ulcers or granulomatous lesions observed on rhinoscopy | 2 |
4 |
| Paranasal sinus involvement | Tenderness or pain over paranasal sinuses (usually confirmed by imaging) | 1 |
2 |
| Subglottic stenosis | Stridor or hoarseness due to inflammation and narrowing of the subglottic area observed by laryngoscopy | 3 |
6 |
| Conductive hearing loss | Hearing loss due to middle ear involvement (usually confirmed by audiometry) | 1 |
3 |
| Sensorineural hearing loss | Hearing loss due to auditory nerve or cochlear damage (usually confirmed by audiometry) | 2 |
6 |
| 5. Chest | Maximum scores | 3 |
6 |
| Wheeze | Wheeze on clinical examination | 1 |
2 |
| Nodules or cavities* | New lesions detected on imaging | * |
3 |
| Pleural effusion / pleurisy | Pleural pain and/or friction rub on clinical assessment; radiologically confirmed pleural effusion. | 2 |
4 |
| Infiltrate | Detected on chest X-ray or CT scan | 2 |
4 |
| Endobronchial involvement | Endobronchial pseudotumor or ulcerative lesions. NB: smooth stenotic lesions to be included in VDI; subglottic lesions to be recorded in the ENT section. | 2 |
4 |
| Massive haemoptysis / alveolar haemorrhage | Major pulmonary bleeding, with shifting pulmonary infiltrates | 4 |
6 |
| Respiratory failure | The need for artificial ventilation | 4 |
6 |
| 6. Cardiovascular | Maximum scores | 3 |
6 |
| Loss of pulses | Clinical absence of peripheral arterial pulsation in any limb | 1 |
4 |
| Valvular heart disease | Clinical or echo detection of aortic / mitral / pulmonary valve involvement | 2 |
4 |
| Pericarditis | Pericardial pain / friction rub on clinical assessment | 1 |
3 |
| Ischaemic cardiac pain | Typical clinical history of cardiac pain leading to myocardial infarction or angina. | 2 |
4 |
| Cardiomyopathy | Significant impairment of cardiac function due to poor ventricular wall motion confirmed on echocardiography | 3 |
6 |
| Congestive cardiac failure | Heart failure by history or clinical examination | 3 |
6 |
| 7. Abdominal | Maximum scores | 4 |
9 |
| Peritonitis | Typical abdominal pain suggestive of peritoneal involvement | 3 |
9 |
| Bloody diarrhoea | Of recent onset | 3 |
9 |
| Ischaemic abdominal pain | Typical abdominal pain suggestive of bowel ischaemia, confirmed by imaging or surgery | 2 |
6 |
| 8. Renal | Maximum scores | 6 |
12 |
| Hypertension | Diastolic >95 mm Hg | 1 |
4 |
| Proteinuria | >1+ on urinalysis or >0.2g/24 hours | 2 |
4 |
| Haematuria | ‘Moderate’ on urinalysis or ≥10 RBC per high power field, usually accompanied by red cell casts | 3 |
6 |
| Serum creatinine 125-249 µmol/L | At first assessment only | 2 |
4 |
| Serum creatinine 250-499 µmol/L | 3 |
6 |
|
| Serum creatinine ≥500 µmol/L | 4 |
8 |
|
| >30% rise in creatinine or >25% fall in creatinine clearance * | Progressive worsening of renal function. Can be used at each assessment if the renal function has deteriorated from prior value | * |
6 |
| 9. Nervous system | Maximum scores | 6 |
9 |
| Headache | Unaccustomed & persistent headache | 1 |
1 |
| Meningitis | Clinical evidence of meningism | 1 |
3 |
| Organic confusion | Impaired orientation, memory or other intellectual function in the absence of metabolic, psychiatric, pharmacological or toxic causes. | 1 |
3 |
| Seizures (not hypertensive) |
Clinical or EEG evidence of aberrant electrical activity in the brain | 3 |
9 |
| Stroke | Focal neurological signs lasting >24 hours due to a CNS vascular event | 3 |
9 |
| Spinal cord lesion | Clinical or imaging evidence of spinal cord involvement | 3 |
9 |
| Cranial nerve palsy | Clinical evidence of cranial nerve palsy – score VIII nerve palsy as sensorineural hearing loss, do not score ocular palsies if they secondary to pressure effects | 3 |
6 |
| Sensory peripheral neuropathy |
Objective sensory deficit in a non-dermatomal distribution | 3 |
6 |
| Mononeuritis multiplex |
Single or multiple specific motor nerve palsies | 3 |
9 |
6)重症度分類としては、EULARでのガイドラインでは下記のEUVASによる重症度分類が使用されている。(Mukhtyar C, et al. Ann Rheum Dis. 2009;68:310-7.)
- 限局型(localized) 上気道病変以外の臓器病変、発熱などの全身症状を認めない病型
- 早期全身型(early systemic):臓器機能あるいは生命に危険を及ぼす病変を伴わないすべての病型
- 全身型(generalized):腎あるいはほかの臓器機能に危険を及ぼす病変を伴う病型。腎病変では血清Cre 5.66 mg/dL未満
- 重症型(severe):腎不全または重要臓器の機能不全を伴う病型、腎病変では血清Cre 5.66mg/dl以上
- 難治型(refractory):ステロイド、シクロフォスファミドに反応しない進行性の病型
7)その他重症度を評価する指標として、Five Factor Score (①年齢>65歳、②心不全、③腎不全(1.7mg/dl)、④消化管病変、⑤ENT病変なし)も使用される(Guillevin L, et al. Medicine (Baltimore). 2011;90:19-27.)。また、現在の活動性による病変だけでなく、非可逆的障害も含めて評価する指標としてvasculitis damage index(VDI)がある。
5.治療
治療は、①寛解導入療法(remission induction)と②寛解維持療法(maintenance)にわけられ、重症度や年齢などに応じて、ステロイド使用量や免疫抑制剤の併用を決定する。一般的には、重要臓器障害がある場合には、高用量ステロイド、ステロイドパルスに加えて、エンドキサンパルス(IVCY)もしくはリツキサン(RTX)を併用して寛解導入を行い、維持療法は少量ステロイドとアザチオプリン(AZP)、RTXを使用することが多い。プロトコールとしては、CYCLOPS(Cyclophosphamide daily Oral versus Pulsed) trial に準じて、IVCY (15 mg/kg, 要腎機能・年齢補正 )を最初の1か月は2週間ごと、続いて3週間ごと合計6か月継続により寛解導入をはかる。9か月後に88%で病状の改善がみられたとされる。RTXの場合は、初回は375mg/m2で4週連続投与を行う。RTXを使用した維持療法については決まったプロトコールはないが、MAINRITSAN studyでは500mg/bodyを6か月ごとに投与している。限局型や早期全身型では中〜高用量ステロイドに加えて、メトトレキサート(MTX)の併用でも病勢コントロールが可能なこともある。病態や治療反応性によっては、血漿交換(MEPEX study)や大量免疫グロブリン療法(IVIg)なども使用されることがある。MMFについてはIMPROVE trial (Hiemstra TH, et al. JAMA. 2010. 304:2381)でAZPより寛解維持の成績が低いことが報告されている。EGPAについては、メポリズマブ(300mg/m)による好酸球抑制が再燃を予防しステロイドを有意に減少させることが明らかとなっている(Wechsler ME, et al. N Eng J Med. 2017.376:1921-32)。
AAVの治療における主要なガイドラインとしては下記のものが挙げられる。
- EULAR/ERA-EDTAのガイドライン(2016年)
- 本邦のガイドライン(2017年)
- BSRとBHPRのガイドライン(2014年)
- ACRガイドライン(2021年)
欧米のガイドラインを参照する際には、欧米と日本でAAVの疫学が異なる点に留意する。
EULAR/ERA-EDTAによるANCA関連血管炎のマネジメントに関する推奨(Yates M, et al. Ann Rheum. Dis. 2016. 75:1583)
- AA患者は専門施設にて、または専門施設と緊密な連携を持って診療されることを推奨する
- 生検での陽性所見は血管炎の診断を強く支持する。新規に診断をつけるため、および血管炎の再燃が疑われる患者の更なる評価のためには生検を推奨する
- 新規発症の臓器障害(organ-threating) または生命に危険が及ぶ( life-threating) AAVの寛解導入には、ステロイドに加えて、シクロフォスファミドまたはリツキシマブの併用が推奨される(A for GPA/MPA, C for EGPA)
- 臓器障害の危険のない(non-organ threating)AAVの寛解導入には、ステロイドに加えて、メトトレキサートまたはミコフェノール酸モフェチルの併用が推奨される(B for MTX, C for MMF)
- 臓器障害(organ-threating) または生命に危険が及ぶ( life-threating) AAVの再燃(major relapse)に対しては、新規発症例と同様に、ステロイドに加えて、シクロフォスファミドまたはリツキシマブの併用が推奨される(A for GPA/MPA, C for EGPA)
- (1)血漿交換は、新規・再燃を問わず、急速進行性腎炎による血清Cre 5.7 mg/dL以上のAAV患者に対して検討されるべきである(B) (2)血漿交換は重症の肺胞出血の治療に考慮される(C)
- AAVの寛解維持には、低用量ステロイドに加えて、アザチオプリン、リツキシマブ、メトトレキサートまたはミコフェノール酸モフェチルの併用が推奨される(A for GPA/MPA, C for EGPA and AZP)
- AAVの寛解維持療法は、寛解導入の後最低24ヶ月の継続が推奨される(D)
- 難治AAVに対する寛解導入療法には、シクロフォスファミドからリツキシマブ、またはリツキシマブからシクロフォスファミドへの変更が推奨される(C)。このような患者については、更なる評価および治験への参加の可能性を考えて、専門施設と緊密な連携して診療を行うか、紹介することが求められる。
- AAVに対する治療を変更する際の判断材料として、ANCA値より構築された臨床評価法(訳注:BVASやVDIなど)を用いるべきである
- シクロフォスファミド投与歴のある患者の原因不明の持続的血尿については、精査を行うことを推奨する
- リツキシマブ投与後に低ガンマグロブリン血症がみられることが知られている。リツキシマブの各コース前、および感染症を反復する際には、血清IgG値を測定することを推奨する
- AAV患者の心血管危険因子について定期的に評価することを推奨する(B)
- AAV患者は、明快な言葉を用いて、疾患の性状、治療の選択肢、副作用、短期および長期予後について説明を受けるべきである。
- 寛解導入後の治療に引き続き、AAV患者は疾患による合併症の程度、持続する影響の評価を受けることを推奨する。どこで必要な治療や支援が受けられるかを、患者に助言すべきである。
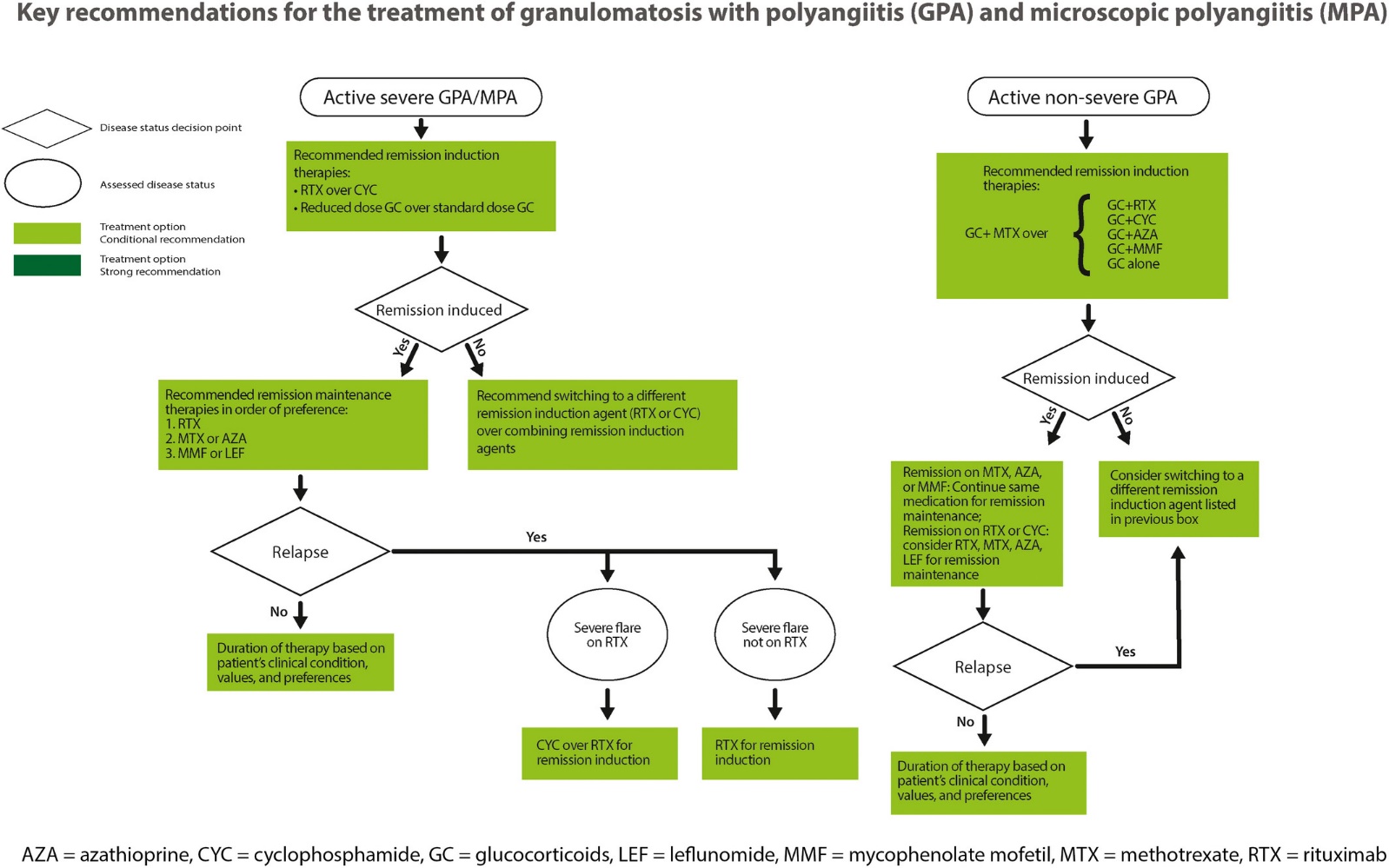
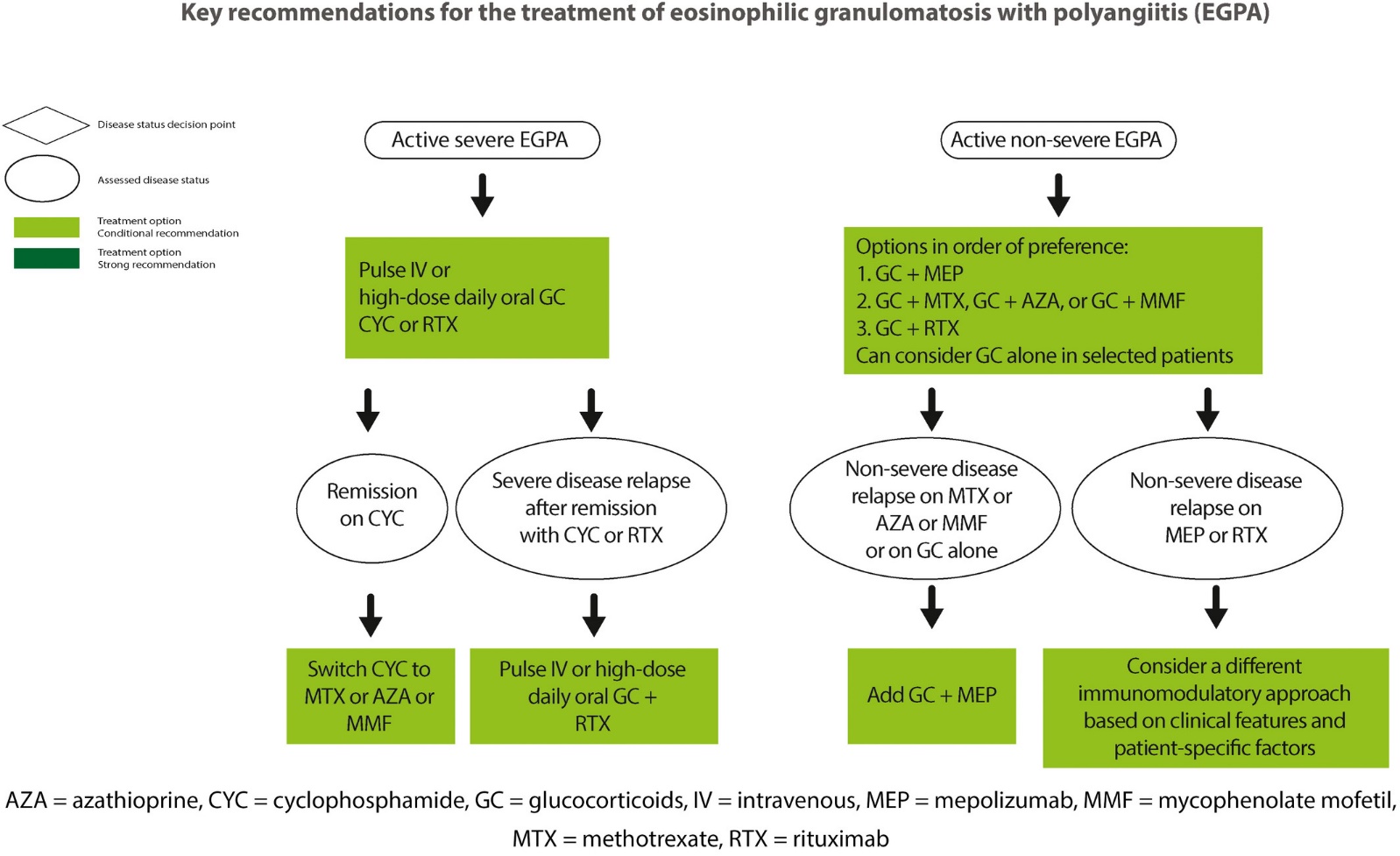
ACRガイドライン(2021年) (Chung SA. Arthritis Care Res. 2021;73:1088-1105)
重症例のGPA/MPAについてはRTX over CYCの推奨となっている。またステロイドに関してはPEXIVAS studyなどで用いられたreduced-dose regimenの推奨が記載されている。
EGPAについては重症例の場合はRTX+GC, CYC+GCが推奨されているが、非重症例の場合は初期治療からのメポリズマブが、MTX, AZPなどの免疫抑制剤と併記されて推奨されている。
6.AAV治療のトピックス
AAV治療に用いるステロイドを減量することが可能という研究結果がでている。
・ステロイド減量プロトコール
GPA/MPAについては初期量ステロイドを0.5mg/kg程度から開始する減量プロトコールで行っても、高容量との治療成績に差がないとの研究報告がなされている。PEXIVAS study (Walsh M. NEJM. 2020;382:622-631)ではESKDをエンドポイントとしてステロイド減量プロトコールの非劣勢が証明されている。LoVAS study (Furuta S. JAMA. 2021;325:2178-2187)は、RTXと併用するステロイドを0.5mg/kgの減量群と1mg/kgの高容量群としてオープンラベルで比較したRCTであり、両群の6か月寛解率に差はなく、減量群で合併症が少なかった。
・アバコパン
アバコパンは経口C5a受容体阻害薬であり、補体C5を介した好中球の活性化を抑制する作用がある。ADVOCATE試験(Jayne DRW. NEJM. 2021;384:599-609)では、免疫抑制剤(RTX, CYC)を併用して、アバコパンとステロイド(PSL 60mg/dayから開始し21週までで減量中止)を比較したRCTで、26週の寛解率は両群に差がなく、52週での寛解維持率はアバコパン群が優れていた。本邦でも2021年に保険収載された。
 東京大学医学部附属病院
東京大学医学部附属病院