疾患解説
皮膚筋炎・多発性筋炎
1. 疾患概念と疫学
特発性炎症性筋疾患(idiopathic inflammatory myositis)は原因不明の筋肉に炎症を生じる疾患群であり、皮膚筋炎、多発性筋炎、封入体筋炎、悪性腫瘍に伴う筋炎、免疫介在性壊死性筋炎などの疾患を含む。臨床的な分類のほかにも、筋炎特異的抗体による分類、病理学的な観点からの分類も試みられている。
- 多発性筋炎(polymyositis: PM);骨格筋、心筋、咽頭筋をおかす特発性炎症性筋疾患。
- 皮膚筋炎(dermatomyositis: DM);同様の筋症状に特徴的な皮膚症状を伴う。
→PMもDMも間質性肺炎などの筋組織以外の内臓病変を伴うことあり。 - 好発年齢;5〜15才と45-65才の二峰性。
- 性差;小児においては性差がないが、成人では女性に多い(男:女性=1:2)。
- 有病率;10万人あたり2人程度。本邦の患者数では17000人(2009年)とされている。
2. 症状と徴候
1)問診のポイント
- 全身症状;発熱、関節痛、レイノー現象、体重減少、筋肉痛、筋力低下、息切れなど
- 日常生活動作
上肢→髪をとかす・重いものを持ち上げるなど、下肢→立ち上がりなど、後頸部筋→枕から頭の持ち上げなど(近位筋症状を尋ねる) - 咽頭筋→嚥下困難、鼻声、構音障害
- 筋痛;約半数でみられる
- 呼吸器症状;労作時息切れ、咳
- 皮膚症状;顔面、手指、爪周囲
- 悪性腫瘍の既往
2)診察のポイント
- 筋力;MMT
下肢の抗重力筋では軽度の筋力低下の場合、医師の手の力よりも強いときがある。椅子からの立ち上がり試験なども有用(Csuka M, McCarty DJ. Simple method for measurement of lower extremity muscle strength. Am J Med. 1985 Jan;78:77)。 - 皮膚所見;診断の項にある“皮膚筋炎のホールマーク皮膚徴候”を参照。Gottron徴候、Gottron丘疹、ヘリオトロープ疹、ショールサイン, mechanic’s handなど。
- 関節所見
- 胸部聴診
3.検査
1)炎症・自己免疫に関わる検査
A,血液検査
- 急性炎症反応(赤沈、CRP);CRPは必ずしも陽転化しない
- 抗核抗体
→抗ARS抗体など一部の筋炎特異抗体が陽性の場合、抗核抗体は細胞質型となる。 - γグロブリン上昇
- 筋炎特異自己抗体
→臨床像との関連がある。 - 抗tRNA合成酵素(ARS)抗体症候群
抗ARS抗体;アミノアシルtRNA合成酵素に対する自己抗体。抗Jo-1抗体、抗PL-7抗体、抗PL-12抗体、抗EJ抗体、抗KS抗体の5つをまとめてELISA法で検出する検査が2014年に保険収載された (参考文献:PLoS One 2013;8:e60442)。抗ARS抗体として、抗Jo-1抗体(抗ヒスチジルtRNA合成酵素抗体)はPMの10-30%で陽性。アラニンtRNA合成酵素(抗PL-12抗体;3%)、スレオニンtRNA合成酵素(PL-7;4%)、イソロイシンtRNA合成酵素(OJ)、グリシンtRNA合成酵素(EJ), アスパラギン酸tRNA合成酵素(KS)などに対する自己抗体も知られている。
抗ARS抗体症候群は、抗tRNA合成酵素抗体が陽性であり、関節炎、間質性肺炎、機械工の手(mechanic's hands)を高率に伴う筋炎の一タイプ。 - 抗Mi-2抗体
CK著明高値で重度の皮疹を伴うことが多い。抗核抗体がhomogeneousかspeckledで高力価となる。 - 抗TIF1抗体
成人では70%以上で悪性腫瘍を認める。しばしば広範囲の浮腫性・炎症性皮疹を伴う。 - 抗MDA5抗体
皮膚症状のみを呈し筋炎症状を欠くDM(=Clinically amyopathic DM=CADM)の一部は抗MDA5抗体陽性である。抗MDA5抗体陽性CADMは短期的な死亡率が高い急速進行性間質性肺炎を伴うため、診断時に間質性肺炎が重症でなくても、期を逃さずに多剤併用療法を開始するべきである。 - 抗SRP(signal recognition particle)抗体陽性壊死性ミオパチー
7SRNAと蛋白との複合体であるSRPを認識する抗体が陽性の多発性筋炎。亜急性の発症経過をとり、治療反応性や機能予後が悪い重症例が多い。心筋や体幹筋もときに障害され、皮疹や間質性肺炎を伴うこともある。壊死性ミオパチーの診断には筋生検が必要。 - 抗HMGCR抗体陽性壊死性ミオパチー
一部はスタチン使用が誘因となって発症する。悪性腫瘍を合併することもある。 - そのほか、研究室でしか検査できないものに、抗NXP-2(MJ)抗体、抗SAE抗体がある。
- 筋炎関連自己抗体として、抗RNP抗体、抗SS-A抗体、抗ミトコンドリア抗体、抗PM-Scl抗体、抗Ku抗体など
2)鑑別に関わる検査
A,血液検査
- 甲状腺機能
- ウイルス検査;コクサッキーB(特にB5・B6)、インフルエンザ、HIV、HBV、EBVなど
3)筋病変に関わる検査
A,血液検査
- CK、CK-MB、CKアイソザイム(マクロCK血症の鑑別)、ミオグロビン、アルドラーゼ、トロポニンT・I、ミオシン軽鎖
CK-MB/CK>25%の場合はマクロCK血症(悪性腫瘍や膠原病に伴う場合もあり)も鑑別。
B,尿検査
- ミオグロビン;ミオグロビン尿では沈査ではRBCを認めずに潜血が陽性となる場合がある。高度の場合にはミオグロビンによる腎障害の精査を。
C,針筋電図
活動性筋炎では安静時放電(fibrillation potentialやpositive sharp wave)はほぼ必発。筋原性疾患間の鑑別よりも神経原性疾患と筋原性疾患の鑑別に有用とされるが、必ずしも両者を鑑別できないこともある。
D,画像
- 骨格筋MRI;脂肪置換・筋萎縮・浮腫・炎症を把握し、診断と生検部位の同定に役立つ。T1WI、T2WI、脂肪抑制T2、STIR、造影MRIなどで撮影。皮膚筋炎では初期より筋膜病変がめだつとされる(Yoshida K, et al Arthritis Rheum. 2010. 62:3751)。
- 骨格筋CT;筋萎縮や肥大、脂肪化、石灰化の評価。炎症は分からない。神経原性疾患、一部の筋ジストロフィーの鑑別に有用。
E,筋生検
- 筋MRI、筋電図所見などを参考に三角筋、上腕二頭筋、大腿四頭筋などを生検する。
- 所見の解釈
(1)炎症細胞浸潤と筋の壊死→壊死周囲細胞の殆どがリンパ球を含まずマクロファージである場合はnecrotizing myopathyや中毒性、ジストロフィーなどを考慮。
(2)ユビキタスなMHCクラスIの発現。→炎症性のジストロフィーとの鑑別に重要。
典型的所見は以下(だが実際は複雑)
|
PM |
DM |
|---|---|---|
炎症細胞浸潤 |
筋線維周囲の筋内膜 |
血管周囲 (membrane attack complexの沈着など) |
筋線維壊死 |
散在性 |
筋束周囲 (perifascicular atrophy) |
F,心筋病変
- 血液検査;上記
- 心電図、Holter心電図;不整脈
- 心エコー
- 心筋MRI;上記検査より心筋障害疑う場合
G,咽頭〜喉頭筋群病変
- 耳鼻科での嚥下評価
- 筋MRI
4)皮膚病変に関わる検査
A,皮膚科診察、皮膚生検. 基底膜の液状変性、真皮のムチン沈着を認める。特にCADMの場合には、皮膚生検は診断に重要とされる。
5)肺病変に関わる検査
A,血液検査
・KL-6、SP-D、SP-A
・動脈血ガス分析、運動負荷時のSpO2(6分間歩行試験)
B,呼吸機能検査;肺拡散能検査も含める
C,肺CT
6)悪性腫瘍に関わる検査
A,胸腹骨盤造影CT
B,上部消化管内視鏡検査、便潜血±下部消化器内視鏡検査
C,男性;年齢によってはPSA、女性;婦人科・乳癌チェック
1994年のメタアナリシス(J Rheumatol. 1994;21:1855)ではodds ratioはPM 2.1、DM 4.4、診断後1年間は5.9、2年目は2.5で、3年目以降は有意な上昇無し。
4.診断
- 診断については、Bohan & Peterによる診断基準が長らく用いられてきたが、2017年に The International Myositis Assessment and Clinical Studies (IMACS) Groupにより筋炎 (idiopathic inflammatory myopathy : IIM) の分類基準 (the EULAR/ACR classification criteria for IIM) が発表された。以下の基準に従い、診断、病型、重症度を評価する。
参考)
Bohan & Peterによる多発性筋炎・皮膚筋炎の診断基準(1975年)
1, 上下肢の対称性の近位筋力低下。
2, 血清筋原性酵素(特にCK)の上昇。
3, 筋電図異常(筋原性病変を示す所見)
4, 筋生検異常(筋の変性,再生,壊死,phagocytosis,間質の単核細胞浸潤)
5, 皮膚筋炎に定型的な皮疹
【診断基準】
多発性筋炎が確実なもの : 1〜4の全項目陽性
多発性筋炎と考えられるもの(probable): 1〜4のうち 3項目陽性
多発性筋炎を除外しえぬもの(possible):1〜4のうち2項目陽性
皮膚筋炎が確実なもの : 5を含め 4 項目以上陽性
皮膚筋炎と考えられるもの(probable) : 5を含め 3項目陽性
皮膚筋炎を除外しえぬもの(possible):5を含め 2項目陽性
→自己抗体・封入体筋炎が考慮されていない
Oslenらによる多発性筋炎・皮膚筋炎の病型分類(1975年)
Ⅰ型 成人の多発性筋炎
Ⅱ型 成人の皮膚筋炎
Ⅲ型 悪性腫瘍を伴う多発性筋炎または皮膚筋炎
Ⅳ型 小児の多発性筋炎または皮膚筋炎
Ⅴ型 他の膠原病を合併した多発性筋炎または皮膚筋炎
119th ENMC international workshopにおける病型分類(2004年:筋病理による分類)
Inclusion body myositis
Definite PM
Probable PM
Definite DM
Probable DM
Amyopathic DM, also called dermatomyositis sine myositis
Possible dermatomyositis sine dermatitis
Nonspecific myositis
Immune-mediated necrotizing myopathy
厚生省特定疾患自己免疫疾患調査研究班による多発性筋炎・皮膚筋炎の診断基準(2015年)
1 .皮膚症状:ヘリオトロープ疹またはゴットロン徴候またはゴットロン丘疹
2 .上肢または下肢の近位筋の筋力低下
3 .筋肉の自発痛または把握痛
4 .血清中筋原性酵素(クレアチンキナーゼ(CK)またはアルドラーゼ)の上昇
5 .筋電図の筋原性変化
6 .骨破壊を伴わない関節炎または関節痛
7 .全身性炎症所見(発熱、CRP上昇、または血沈亢進)
8 .抗ARS抗体 陽性(抗Jo-1抗体を含む)
9 .筋生検で筋炎の病理所見:筋線維の変性および細胞浸潤
【診断基準】
皮膚筋炎
1と2から9の項目中4項目以上
多発性筋炎
2〜9の項目中 4項目以上
鑑別:感染による筋炎、薬剤・内分泌異常に基づくミオパチー、筋ジストロフィー、先天性筋疾患、他の皮膚疾患
Sontheimerにより提案されたclinically amyopathic dermatomyositis(CADM)の定義
(皮膚症状出現からの期間は問わない) (J Am Acad Dermatol 2002; 46(4): 626-36.)
Amyopathic dermatomyositis
皮膚生検により確証された皮膚筋炎のホールマーク皮膚徴候があり、6ヶ月以上近位筋力低下および筋酵素活性異常がないもの。それら以外の筋評価が行われた場合は、結果は正常範囲内。
以下の場合は除外
・皮膚病変発症から6ヶ月以内に全身性免疫抑制治療が連続する2ヶ月以上行われた場合
・皮膚病変出現時にHydroxyureaなど皮膚筋炎によく似た病変をおこしうる薬剤使用あり
Hypomyopathic dermatomyositis
皮膚筋炎に特異的な皮膚所見を持つ患者で、筋力低下などの筋疾患の臨床的証拠がないもので、血液検査、筋電図、それと/または、放射線学的評価において臨床的に意義のある筋炎の証拠としては満たさない結果しかえられないもの
Clinically amyopathic dermatomyositis
上記の両者を含むもの。
皮膚筋炎のホールマーク皮膚徴候の定義
大基準;ヘリオトロープ疹、Gottron丘疹、Gottron徴候
小基準;斑状紫紅斑、爪周囲および爪床の毛細血管拡張または爪上皮における出血・梗塞、多型皮膚萎縮症、機械工の手、皮下石灰化、皮膚潰瘍、掻痒症
(斑状紫紅斑;頭皮・前頭部毛髪線、顔面の頬部隆起・前額部・顎、前頚部のV領域または上胸部(V徴候)、首筋・肩の背面(ショール徴候)、上腕または前腕の伸側、手背の伸筋腱に沿った直線状の筋、爪周囲、大腿または臀部の外側面(ホルスター徴候)、内果)
大基準2項目、大基準1項目および小基準2項目以上をみたし、皮膚病変の少なくとも一つにおいて皮膚生検が行われ皮膚筋炎の皮膚病変に合致する所見を呈する場合、皮膚筋炎のホールマーク皮膚徴候が存在するとする。
the EULAR/ACR classification criteria(参考文献:Ann Rheum Dis 2017; 76: 1955-1964.)
The International Myositis Assessment and Clinical Studies (IMACS) Groupが、研究や臨床試験で使用できるようvalidatedされた筋炎 (idiopathic inflammatory myopathy : IIM) の分類基準 (the EULAR/ACR classification criteria for IIM) を発表した。
下記の表1のように項目毎にscoreが割り振られており、scoreの合計 からprobability of IIM (%) を算出でき、その値が90%以上なら”definite IIM”、55%以上90%未満なら“probable IIM”、50%以上55%未満なら”possible IIM”、50%未満なら”rule out IIM”と判定される。probabilityが55%以上(definiteまたはprobable)の場合、図1に従ってIIMの亜分類を行う。probabilityの計算を簡単に行えるようweb siteが用意されている。(www.imm.ki.se/biostatistics/calculators/iim)
表1:分類基準における各項目のscore
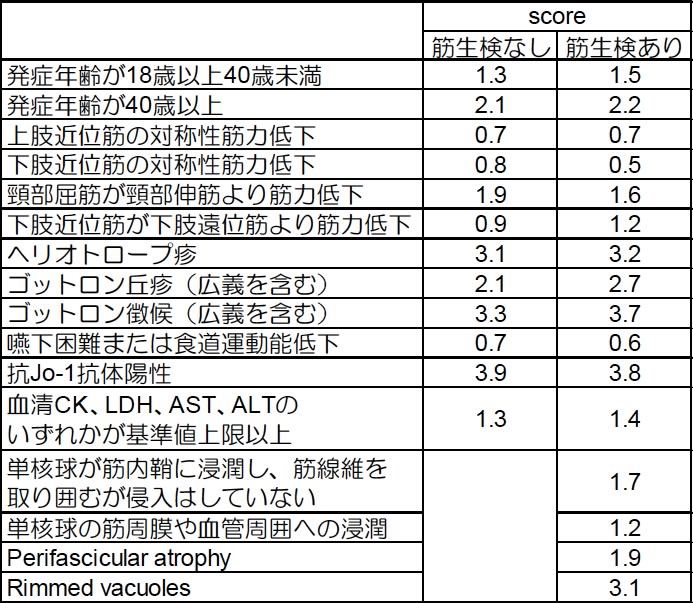
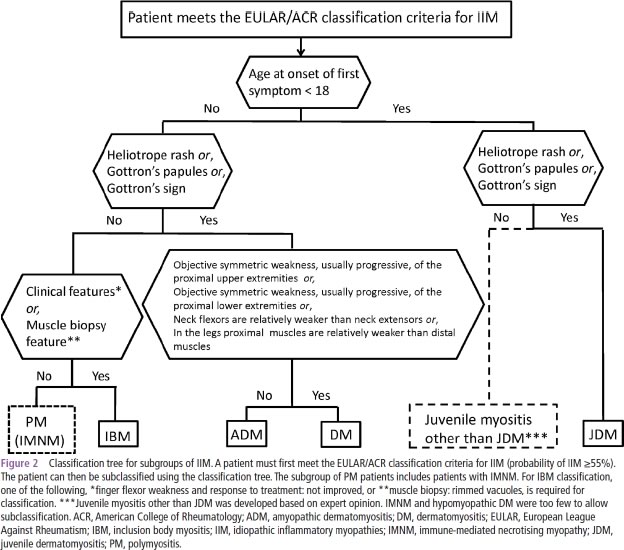
図1:筋炎の亜分類基準
- Probability 55%以上(definiteまたはprobable)を”IIMである”と判定する場合、初診時にIIMが鑑別にあがった症例群からIIMを弁別する感度、特異度はいずれも高く、専門医が総合的に診断した結果を正診とした場合の感度・特異度は、筋生検をした場合 93%・88%、筋生検をしていない場合 87%・82%である。
- ヘリオトロープ疹、ゴットロン丘疹/徴候、抗Jo-1抗体は特にscoreが高い。すなわちこれらが存在すればIIMの可能性がより高まると考えられる。
- 「特徴的な皮疹がない場合は筋生検をすべき、CADMの場合は皮膚生検すべき」と明記されている。
- 本基準で用いた患者群におけるアジア人の割合は976例中177例(18.1%)と多くない。壊死性筋症やhypomyopathic DM、小児PMは、症例数が少なかったため、図1の亜分類には含まれていない。また、抗Jo-1抗体以外の筋炎特異抗体についても、あれば診断価値が高いが、陽性例が少なかったためscore化できていない。さらなる症例の蓄積が待たれる。
5. 治療
1)寛解導入時の治療
- 心筋・呼吸筋・咽頭筋障害・高度の骨格筋筋力低下、壊死性ミオパチーの場合は、ステロイドパルスを考え、早期よりMTX、Tac等の併用やIVIGも検討する。
- 初期ステロイド治療はPSL 1〜1.2mg/kg/dayが基本。CK<500程度で筋力低下がごく軽度の軽症例ではPSL 0.6〜0.8mg/kg/dayで治療開始する場合もある。
- 悪性腫瘍合併時には、悪性腫瘍の治療が優先。腫瘍治療後も筋炎の改善を認めない場合はステロイド治療を考慮する。
2)ステロイド治療への反応性をどう考えるか?
- CK値が2週間で50%以上改善している場合は順調と考える(Mastaglia, J Clin Neurosci. 2003:10:99)。筋力改善は改善まで時間を要することが多い。
- CKの低下は重要だが、筋力が改善しない場合は、活動性の残存、ステロイドの影響、リハビリテーションの必要性などに注意しつつ、免疫抑制剤、IVIGなどの追加治療を考慮する。
- 治療効果が全くない場合は、封入体筋炎、necrotizing myopathy、成人発症筋ジストロフィーなど診断を再考する必要がある。
3)減量はどのように行うか?
- 上記ステロイド反応性が得られていれば初期量4週間で減量に入ることが多い。1〜2週間で10〜15%程度の減量を行う。最終的にはPSL 5mg/day前後が維持量となることが多いが、再燃も稀ではなく、ステロイド維持量減量を目的としたTac, MTX, AZPなどの免疫抑制剤併用が考慮される。
4)治療抵抗性の場合はどうするのか?
- 反応性不良と考える場合は、MTXやCyA、TAC、AZAの併用。MTX+CyA、MTX+AZAも行われる。IVIGもこれらの治療が効果を認めない場合には考慮される。
- これらの免疫抑制剤は、反応不良時、ステロイドの一時的強化(ステロイドパルス療法や50〜100%程度の増量)とともに開始することが多い。
- 高用量ステロイドと少なくとも1種の免疫抑制剤による治療で改善不十分な多発性筋炎、皮膚筋炎にRTXを使用したところ、44週の経過で83%が臨床的に改善したとの報告がある。(参考文献:Arthritis Rheum 2013; 65(2): 314-24.)
- 他に、成人・小児の皮膚筋炎による難治性皮疹にRTXが有用との報告や、小児皮膚筋炎の筋症状にRTXが有用との報告がある。
(参考文献:Rheumatology 2017; 56(2): 247-254.、J Rheumatol 2011; 38(7): 1436-40.) - CKの再上昇はなくとも治療中に筋力低下が進行もしくは改善しない場合は、活動性残存以外にステロイド筋症の可能性も考える。
5) CADMの治療について
- CADMに対しては治療開始時より多剤併用療法が基本。高用量ステロイド(ステロイドパルス含む)、IVCYとカルシニューリン阻害薬を併用した治療を行う。抗MDA5抗体陽性CADMの場合、フェリチン値や抗MDA5抗体価が予後不良および疾患活動性のマーカーとして有用である。難治例では血漿交換やrituximab(RTX)が使用される。(参考文献:Mod Rheumatol 2017; 27(3): 536-540.)
平成 30年 5月
 東京大学医学部附属病院
東京大学医学部附属病院








